Douleurs abdominales, ballonnements, diarrhée et constipation… Le syndrome de l’intestin irritable (ex : la colopathie fonctionnelle) est un motif de plainte récurrente au comptoir. Sa prise en charge thérapeutique était au cœur des Rencontres de l’Officine. Retour d’expérience et de cas concrets pour aider ces patients en quête d’écoute et d’orientation !
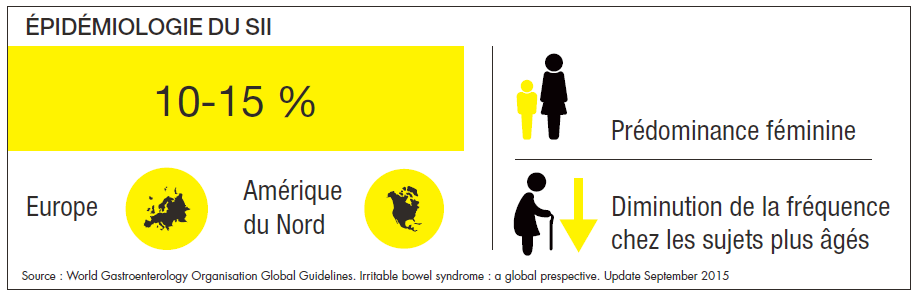
Près de 15 % de la population, en a déjà souffert. Soit 8,5 millions de Français, et surtout de Françaises ! Le syndrome de l’intestin irritable (SII) est un vrai désordre encore difficilement reconnu et diagnostiqué par le corps médical, mais classé dans les troubles digestifs fonctionnels. Il touche en moyenne deux femmes pour un homme avec un pic de fréquence entre 25 et 55 ans… Soit autant de patients susceptibles de vous demander conseil au comptoir.
Un mal sournois et polymorphe
Le SII est caractérisé par des douleurs abdominales récurrentes, bien souvent associées à des problèmes digestifs comme des diarrhées et/ou une constipation. Plus ou moins intenses, ces douleurs sont décrites par les patients comme des « spasmes douloureux », « l’impression que le ventre se tord » ou « des bulles qui éclatent dans le ventre ». La chronicité est un élément clé, avec une récurrence d’au moins un jour par semaine au cours des trois derniers mois. Pour confirmer un SII, l’ensemble des signes doit être présent depuis au moins 6 mois. Par ailleurs, les symptômes s’accompagnent également très fréquemment de ballonnements, flatulences et gaz1, selon les critères de Rome.
Le diagnostic est avant tout un diagnostic d’élimination, compte tenu de l’absence de test pour établir avec certitude le SII. Il ne peut être posé par le médecin qu’après vérification par coloscopie ou d’autres examens que le côlon est normal et qu’aucune maladie digestive n’est présente. Pour ne pas risquer de passer à côté d’une pathologie grave, questionnez toujours un patient se plaignant de douleurs abdominales sur la présence ou non de sang dans les selles et d’antécédents de cancer digestif dans la famille. Ce type de symptôme peut en effet refléter un cancer du côlon, du rectum ou évoquer une maladie inflammatoire chronique de l’intestin (MICI) telle que la maladie de Crohn ou la rectocolite hémorragique2. Toute évolution soudaine du transit et altération de l’état général doit également donner lieu à une consultation du médecin généraliste, voire dugastro-entérologue. N’hésitez donc pas à réorienter le patient vers son médecin traitant. Il est essentiel qu’un diagnostic d’exclusion soit impérativement fait avant d’évoquer un SII.
Un déséquilibre du microbiote intestinal, ou dysbiose, est très souvent constaté chez les patients souffrant de SII. Ils présentent une réduction de la quantité ou de la variété des bacteries. Une importante perte de la diversité bactérienne est aussi retrouvée dans les MICI du tube digestif avec pour conséquences des anomalies de la barrière, une dysfonction immunitaire, une hypersensibilité viscérale et des troubles de la motilité. Cette dysbiose modifie la barrière intestinale en la rendant perméable. « On s’est rendu compte qu’il existe une translocation bactérienne (passages des bactériespartant de l’intestin vers l’organisme) et cette hyperperméabilité digestive créé une microinflammation chronique » explique le Dr Anne-Laure Tarrerias, gastroentérologue à Paris et intervenante lors des Rencontres de l’Officine en mars dernier. Le SII pourrait donc être expliqué par ce phénomène et une chose est sûre : le microbiote a le plus souvent une importance dans la genèse de ces symptômes.
 Une qualité de vie altérée, des besoins thérapeutiques insatisfaits
Une qualité de vie altérée, des besoins thérapeutiques insatisfaits
Si le SII n’est pas une maladie grave, il n’en reste pas moins handicapant au quotidien et altère de façon significative la vie professionnelle et sociale. Sa répercussion entrainerait en moyenne 3,2 jours d’arrêt de travail par an et par personne. Les patients l’expriment clairement avec le sentiment de souffrir, sans parfois trouver de réels soutiens : « ça me gâche la vie », « C’est gênant au travail », ou encore « Personne ne me comprend, on me dit que c’est dans la tête » sont autant de verbatims recueillis3. Beaucoup arrivent au comptoir en quête d’écoute et d’une solution efficace pour apaiser leurs symptômes.
Principal problème : si les symptômes peuvent être soulagés ponctuellement par des antispasmodiques, des laxatifs ou des antidiarrhéiques, le problème de fond lui reste. D’où la récurrence du SII et les douleurs qui reviennent. « Beaucoup de patients prennent ces médicaments depuis des mois, mais arrivent au comptoir en quête d’autres traitements plus efficaces, pour soulager ou espacer les crises et améliorer leur qualité de vie » indique Béatrice Clairaz, pharmacienne à Châtenay-Malabry et coanimatrice de la conférence. Les traitements pharmacologiques à visée symptomatique englobent aussi les régulateurs de transit auxquels il faut généralement souvent associer des antalgiques de palier I en raison des nombreux symptômes périphériques.
Une vaste prise en charge à la fois pharmacologique et non pharmacologique
La prise en charge du SII peut également passer par des traitements non pharmacologiques en modifiant l’hygiène de vie4. La grande majorité des patients souffrant de SII sont stressés et souffrent en parallèle de troubles du sommeil. Il faut savoir les dépister au comptoir. De la mélatonine peut ainsi leur être délivrée. Conseillez-leur également les thérapies cognitives et comportementales (TCC), ainsi que les techniques de relaxation comme l’hypnose5, qui, testée lors d’études cliniques, a donné de bons résultats. La nutrition est elle aussi une solution prometteuse. Parmi les plaintes de patients, nombreux disent ne plus savoir quoi manger et ont peur que certains aliments n’aggravent leur état. Certains, rapportant une hypersensibilité non cœliaque au gluten, l’ont d’emblée exclu de leur alimentation. Mais d’après les études menées, le régime sans gluten semblerait ne pas avoir prouvé son efficacité, malgré l’engouement actuel qu’il suscite.
Les espoirs se tournent en revanche vers le régime sans Fodmaps (voir encadré). Le Dr Tarrerias, souligne que « des études à très fort niveau de preuves ont été publiées récemment en gastroentérologie, les seules qui soient randomisées et contrôlées, régimes placebo à l’appui ». Près de 61 % des patients souffrant de SII mis au régime sans Fodmaps pendant 6 à 12 semaines voyaient leurs symptômes s’améliorer, mais certains font des erreurs diététiques sans s’en rendre compte. D’autre part, si un tube digestif mis au repos va vite mieux, la reprise des aliments incriminés peut également s’avérer problématique. « Il est intéressant de faire passer comme messages qu’il y a d’autres alternatives » précise Béatrice Clairaz.
Le rôle essentiel du microbiote
Compte tenu de la fréquence de la dysbiose6 retrouvée chez les patients souffrant de SII, pas étonnant que les probiotiques occupent une place de plus en plus importante dans sa prise en charge7. Une option parfois plus simple à suivre au quotidien et dont vous devez aujourd’hui parler aux patients en chassant les idées reçues que certains peuvent avoir sur le sujet !
Pour rappel, le microbiote intestinal remplit des fonctions métaboliques essentielles comme la synthèse des vitamines, la fermentation des résidus ou encore absorption d’ions… Ce qu’on appelait autrefois la flore intestinale sert aussi de barrière immunologique et de protection. Son rôle essentiel : nourrir et protéger. Un microbiote « normal » renferme une population de bactéries diverse et bien équilibrée entre celles dites bénéfiques (Lactobacilles et bifidobactéries) et d’autres nuisibles (Clostridium, Collibacilles, Salmonelles et Pseudomonas). Un maintien du bon état physiologique préserve cette harmonie. L’antibiothérapie va au contraire déséquilibrer la flore intestinale en diminuant le nombre de bonnes bactéries.
Comment bien conseiller et choisir les probiotiques ?
Pour répondre aux attentes des patients souffrant de SII, les probiotiques contiennent des êtres vivants devant être conditionnés à un dosage approprié jusqu’à la date de péremption, avec une variabilité minimale d’un lot à l’autre. Ils doivent également être spécifiés par genre et par souche. Autre exigence : avoir fait la démonstration de leur efficacité et de leur sûreté chez l’homme dans des études cliniques contrôlées (voir encadré). Oui, mais comment choisir la bonne souche ? C’est la vraie question, alors qu’il existe aujourd’hui environ 300 espèces et des milliers d’espèces rien que pour le Lactobacille ! Tous les probiotiques ne se valent pas. L’essentiel est de ne recommander que ceux qui ont fait leurs preuves.
Le collège Américain de gastro-entérologie8 a analysé l’ensemble des essais cliniques disponibles et conclut finalement que très peu de souches correspondent aux recommandations publiées en 2014. Seules trois souches sont conseillées, mais une seule d’entre elles est disponible en France et à la bonne dose : le Lactobacillus plantarum 299v.
Globalement, il reste difficile de bénéficier des informations nécessaires pour conseiller un probiotique plutôt qu’un autre. Demandez à voir les études publiées, randomisée chez l’Homme et à la dose commercialisée. Allez à la pêche aux informations. N’hésitez pas à regarder leur composition avant de les délivrer (quantité de bactéries disponibles et garantie jusqu’à péremption). Les probiotiques sont sensibles à l’acidité gastrique donc, mieux vaut ne pas ouvrir la gélule. Certains existent également en sachets pour l’enfant. Sachez enfin que des progrès rapides sont à prévoir dans les prochaines années. Peut-être enfin une thérapeutique d’avenir pour mieux soigner le SII !
-
Lacy B E et al. Bowel Disorders. Gastroenterology 2016 ; 150:1393–1407
-
SNFGE. GFNG. Sabaté JM, Jouët P. Conseil de pratique. Prise en charge du Syndrome de l’Intestin Irritable (SII). 19 septembre 2016.
-
http://www.apssii.org/accueil/index.php
-
SNFGE. GFNG. Sabaté JM, Jouët P. Conseil de pratique. Prise en charge du Syndrome de l’Intestin Irritable (SII). 19 septembre 2016.
-
Peters et al, Review article: gut directed hypnotherapy in the management of irritable bowel syndrome and inflammatory bowel disease, Aliment PharmacolTher 2015; 41: 1104–1115.
-
Casen C et al, Deviations in human gut microbiota: a novel diagnostic test for determining dysbiosis in patients with IBS or IBD. Aliment Pharmacol Ther 2015; 42 : 71–83.
-
Valerio Mezzasalma, et al. A randomized, double-blind, placebo-controlled trial: the efficacy of multispecies probiotic supplementation in alleviating symptoms of irritable bowel syndrome associated with constipation, BioMed Reasearch International, volume 2016, Article ID 4740907
-
Ford AC et al, American College of Gastroenterology Monograph on the Management of Irritable Bowel Syndrome and Chronic Idiopathic Constipation. Am J Gastroenterol. 2014 ; 109 Suppl 1:S2-26.
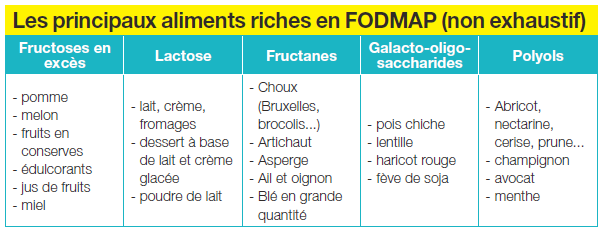
Zoom sur le régime FODMAP
Le régime FODMAP*, pour Fermentable Oligo-, Di-, and Monosaccharides, And Polyols, est l’une des pistes thérapeutiques pour limiter les symptômes du SII. Récent et peu connu, il concerne les hydrates de carbone à courtes chaines et produits non fermentescibles, essentiellement des sucres, qui, une fois ingérés, arrivent directement dans le côlon et font l’objet de fermentation et de ballonnements. Seul problème : on retrouve les Fodmaps à peu près partout dans l’alimentation, dans de nombreux fruits et légumes, les laitages, les céréales… et même les édulcorants. ! Très difficile à suivre, ce régime d’exclusion doit être encadré par un médecin nutritionniste ou une diététicienne et suivi sur du court terme, soit 1 à 2 mois, au risque d’induire des carences en calcium et protéines. La réintroduction est progressive et le patient essaie de repérer les aliments qu’il ne tolère pas. Après un régime FODMAP, 6 à 18 mois après la reprise d’une alimentation équilibrée, 70 % des patients allaient toujours aussi bien, tandis que 30 % rechutaient. Ceux chez qui la diététique n’avait pas marché étaient au contraire seulement 38 % à constater une amélioration.
*Magge S et al. Low-FODMAP Diet for Treatment of Irritable Bowel Syndrome. Gastroenterology & Hepatology Volume 8, Issue 11 November 2012 – Gastroenterology 2013 ; 145:320-328. Biesiekierski et coll
Quels critères pour définir un bon probiotique ?
En 2011, la World Gastro-enterology Organisation* a mis au point les 5 critères essentiels de qualité d’un probiotique :
- il doit être spécifié par type, souche et genre
- il doit être vivant : c’est le nombre d’unités formant colonies (UFC)
- il doit être conditionné à un dosage approprié qui reste stable jusqu’à la date de péremption et avec une variabilité minimale d’un lot à l’autre
- il doit avoir démontré son efficacité dans des études contrôlées chez l’Homme, à la dose commercialisée
- il doit être sûr pour les usages prévus.



 Une qualité de vie altérée, des besoins thérapeutiques insatisfaits
Une qualité de vie altérée, des besoins thérapeutiques insatisfaits